"Panie Mariuszu - jak można Pana wesprzeć?" - zadał mi pytanie jeden z moich subskrybentów. Blog na Substacku jest to hobby czasochłonne, ale nie planowałem tej działalności, jako źródła dodatkowego dochodu (do tej pory mam jednego płatnego subskrybenta ochotnika). Ale jeśli ktokolwiek uważa, że warto udzielić mi wsparcie finansowe - to poniższa zrzutka daje taką możliwość. Za każdą wpłatę - serdecznie dziękuję :)
„Nie bierz się do czytania badań gdy są za trudne” radzi mi Olek (@ikaniewicz) w odpowiedzi na mój tweet, który był tłumaczeniem wpisu autorstwa @dchomecoming, na który uwagę zwróciła Brook Jackson. Niejaki Magic – the crypto noob (@MaciekTarr) dodaje, że „dokument źródłowy mówi ci(o?) innego".
Treść umieszczonego tłumaczenia: „W badaniach klinicznych Pfizera uczestniczyło 44.000 uczestników ale liczba dawek szczepionki mRNA została zatwierdzona w oparciu podstawie 170 uczestników. Z tych 170-162 otrzymało placebo, a 8 otrzymało 2 dawki mRNA. W ten sposób Pfizer twierdzi, że osiągnął 95% skuteczności.” Wpis był dużym uproszczeniem – sam autor go usunął – ale sprawdźmy o co chodzi z 95% skutecznością szczepionki i 170 osobami.
W kwietniu 2021 The Lancet publikuje artykuł „Skuteczność i efektywność szczepionki COVID-19 – słoń (nie) w pokoju” https://www.thelancet.com/action/showPdf?pii=S2666-5247%2821%2900069-0, w którym pojawiają się terminy efficacy i effectiveness, które często są używane zamiennie, a które odnoszą się do czegoś zupełnie innego. Zwrócono na to uwagę w opublikowanym we Frontiers in Molecular Immunology (Podstawy immunologii molekularnej) artykule naukowo-badawczym „Parametry skuteczności i bezpieczeństwa nowej szczepionki COVID-19” autorstwa Bożeny Riedel-Baima, Romana Zielińskiego i Kornelii Polok - https://www.syncsci.com/journal/FMI/article/view/521/430. Autorzy piszą: „Istnieje różnica między skutecznością a efektywnością, która jest zbyt często ignorowana, a słowa te są często używane zamiennie. Skuteczność (Effectiveness) opisuje sposób stosowania leku w warunkach rzeczywistych, gdzie nie można kontrolować populacji pacjentów i innych zmiennych. Efektywność (Efficacy) opisuje, jak lek działa w wyidealizowanym lub kontrolowanym otoczeniu - mianowicie w badaniu klinicznym. Badania skuteczności nie są tym samym, co badania efektywności.” W konkluzji autorzy twierdzą, że „błędne rozumienie terminu „skuteczności” wpływa na politykę zdrowia publicznego w wielu krajach, np. w Niemczech na "formularzu zgody na szczepienie" dla pacjentów znajdujemy następujące wyjaśnienie: "Zgodnie z obecnym stanem wiedzy ok. 95 na 100 zaszczepionych osób jest chronionych przed zachorowaniem" co nigdy nie zostało zbadane. Sami autorzy badań klinicznych, być może niezamierzenie, mogą sugerować taką interpretację, pisząc we wnioskach " Schemat dwóch dawek BNT162b2 zapewniał 95% ochronę przed Covid-19 u osób w wieku 16 lat i starszych". Ponadto, w miarę jak praca była tłumaczona na inne języki, słowo "efficacy" (efektywność) mogło być mylone ze słowem "effectiveness” (skuteczność działania).”
Wróćmy do The Lancet – autorzy w artykule piszą: „Skuteczność szczepionki jest często podawana jako względne zmniejszenie ryzyka (RRR). Wykorzystuje się tu ryzyko względne (RR) - tzn. stosunek liczby zachorowań z użyciem szczepionki i bez niej - które wyraża się jako 1-RR. Ranking według zgłoszonej skuteczności daje względne zmniejszenie ryzyka o 95% w przypadku szczepionek Pfizer-BioNTech, 94% w przypadku szczepionek Moderna-NIH, 91% w przypadku szczepionek Gamaleya, 67% w przypadku szczepionek J&J i 67% w przypadku szczepionek AstraZeneca-Oxford. Jednak RRR należy rozpatrywać w kontekście ryzyka zakażenia i zachorowania na COVID-19, które jest różne w różnych populacjach i w różnym czasie. RRR uwzględnia tylko uczestników, którzy mogliby odnieść korzyści ze szczepienia, bezwzględne zmniejszenie ryzyka (ARR), czyli różnica między liczbą zachorowań przy zastosowaniu szczepionki i bez niej, dotyczy całej populacji. ARR są zwykle ignorowane, ponieważ dają znacznie mniej imponującą wielkość efektu niż RRR: 1-3% dla szczepionki AstraZeneca-Oxford, 1-2% dla szczepionki Moderna-NIH, 1-2% dla szczepionki J&J, 0-93% dla szczepionki Gamaleya i 0-84% dla szczepionki Pfizer-BioNTech.”
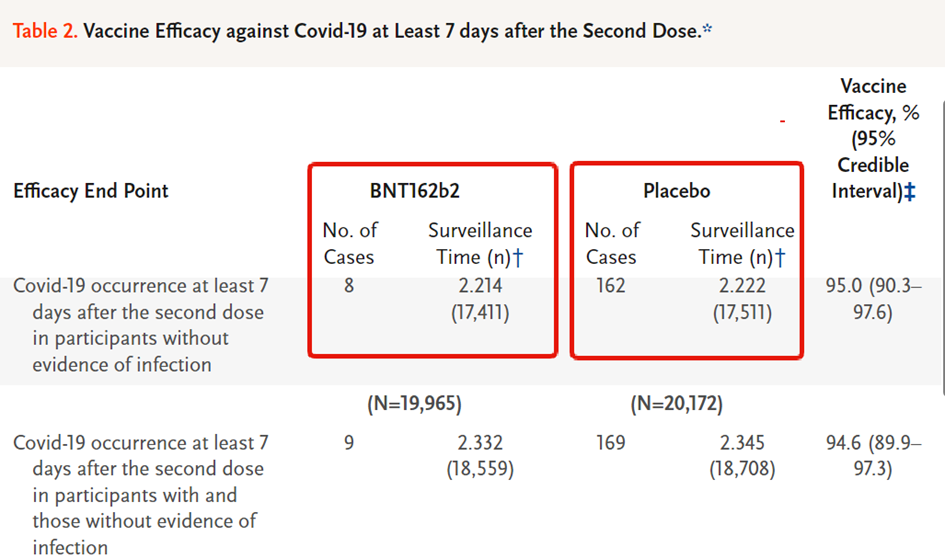
Te 95% odnosi się do 'względnego zmniejszenia ryzyka' (RRR), ale nie mówi o tym, jak bardzo ogólne ryzyko jest zmniejszone przez szczepienie. Do tego potrzebne jest 'bezwzględne zmniejszenie ryzyka' (ARR). W badaniu przeprowadzonym przez firmę Pfizer u 8 z 18 198 osób, którym podano szczepionkę, rozwinęła się choroba COVID-19. W nieszczepionej grupie placebo (18 325 osób) zachorowały 162 osoby, co oznacza, że nawet bez szczepionki ryzyko zachorowania na COVID-19 było niezwykle niskie i wynosiło 0,88%, a szczepionka zmniejszyła je do 0,04%. Tak więc korzyść netto, bezwzględne zmniejszenie ryzyka, które oferuje szczepionka firmy Pfizer, wynosi 0,84%. Liczba 95% odnosi się do względnej różnicy między 0,88% a 0,04%. To jest nazywane „95% redukcją ryzyka względnego”. A względna redukcja ryzyka jest dobrze znana jako liczba wprowadzająca w błąd, (nawet FDA zaleca stosowanie bezwzględnej redukcji ryzyka). Co rodzi pytanie: Ile osób zdecydowałoby się na przyjęcie szczepionek COVID-19, gdyby zrozumieli, że oferują one mniej niż 1% korzyści?”. W listopadzie 2020 pisał o tym Peter Doshi – jeden z wydawców British Medical Journal - https://blogs.bmj.com/bmj/2020/11/26/peter-doshi-pfizer-and-modernas-95-effective-vaccines-lets-be-cautious-and-first-see-the-full-data/, zwracają na to także autorzy wspomnianego badania „Efficacy and safety parameters of a novel COVID-19 vaccine” - Bozena Riedel-Baima, Roman Zielinski i Kornelia Polok: https://www.syncsci.com/journal/FMI/article/view/521/430.
Dane o skuteczności pochodzą ze sprawozdania, które 31 grudnia 2020 Pfizer opublikował w New England Journal of Medicine (https://www.nejm.org/doi/full/10.1056/NEJMoa2034577), w którym przedstawił dane dotyczące bezpieczeństwa i skuteczności, zebrane z 2 miesięcy badań. Jak już wspomniałem opisano przypadki 43,548 osób podzielonych na 2 grupy: leczoną (otrzymała szczepionkę) i kontrolną (która otrzymywała sól fizjologiczną), obserwacja trwała 2 miesiące, a celem było sprawdzenie, u kogo rozwinął się COVID-19. W wyniku badań stwierdzono, że szczepienia były bezpieczne i wykazywały 95% skuteczności 7 dni po podaniu drugiej dawki. Podczas badań klinicznych jedynie 8 (osiem) osób spośród 18 198 badanych wśród grupy szczepionej zachorowało na Covid-19, w grupie placebo było to 162 spośród 18 325 badanych.
Badania Pfizera nie przebiegały jednak zgodnie z zaplanowaną procedurą. Badanie randomizowane zostało zbyt wcześnie odślepione i nie gromadzono długoterminowych danych dotyczących bezpieczeństwa.
W założeniach plan był taki: badane miały być 2 grupy – szczepiona i placebo – obie po około 21 000 ochotników. 3 faza badań klinicznych rozpoczęła się 27 lipca 2020. Badanie było zaślepione – nikt z uczestników nie wiedział w której grupie się znajduje oraz miało trwać przez 3 lata i zakończyć się w maju 2023 – ta data miała kończyć 3 fazę badań klinicznych, i wtedy powinno nastąpić odślepienie badania i dopiero wtedy grupa placebo mogła zostać zaszczepiona, jeśli tego by chciała bądź wymagała. Realizacja wyglądała zupełnie inaczej. Po zgromadzeniu danych z 2 miesięcy badania, odślepiono je, informując uczestników do jakiej grupy byli przypisani, oferując grupie placebo przejście do grupy osób szczepionych – z czego skorzystała olbrzymia większość uczestniczących w badaniu. Oznacza to, że pozbawiono się grupy kontrolnej już na początku 2021 i w trakcie 3 fazy badań klinicznych nie będzie można oszacować skuteczność długoterminowej szczepień oraz kwestii bezpieczeństwa.
Pierwszym autorem publikowanego w NEJM badania był Fernando P. Polack. Z dokumentów ujawnionych przez FSA po przegranej w sądzie w Teksasie (FDA wnioskowało o 75 lat na ujawnienie całości dokumentacji, na podstawie której udzielono tymczasowej autoryzacji dla szczepionek Pfizer/BioNTech - co zajęło agencji 108 dni) wynika, że zdecydowanie największym rekruterem chętnych do badań klinicznych był ośrodek o numerze 1231, mieszczący się w Argentynie, Hospital Militar Central, a osobą odpowiedzialną za badania był właśnie Fernando Polack. Ośrodek ten zrekrutował 4501 chętnych czyli ponad 10% pacjentów całego badania – a to tylko jeden ośrodek spośród 153 placówek. Wszyscy pacjenci zostali zrekrutowani w ciągu zaledwie 3 tygodni. Kim jest dr Fernando Polack? Jego życiorys złożony dla potrzeb badań klinicznych jest dostępny na pierwszej stronie tego dokumentu: https://www.icandecide.org/wp-content/uploads/2022/03/Pages-42-289-Section-5.2-listing-clinical-sites-cvs_Part-A.pdf. Wynika z niego, że Fernando Polack jest osobą niezwykle zajętą – poza prowadzeniem badań klinicznych na zlecenie Pfizer na oddziale macierzyńskim i dziecięcym szpitala wojskowego w Argentynie, jest także wykładowcą na Uniwersytecie Vanderbilt w Nashville w stanie Tennessee w USA, pracuje w The Infant Foundation (http://infant.org.ar), która jest finansowana przez Bill & Melinda Gates Foundation oraz NIH. Jest także konsultantem przy FDA. Jak Pan doktor znalazł także czas, żeby być głównym autorem badania „Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine”?
Badania kliniczne prowadzone były w 153 placówkach (firmach komercyjnych i ośrodkach akademickich), które łącznie stworzyły 270 klinicznych ośrodków rekrutacyjnych, ponumerowanych kolejno od 1001 do 1270 (pełna lista https://www.icandecide.org/wp-content/uploads/2022/03/5.2-listing-of-clinical-sites-and-cvs-pages-1-41.pdf), gdzie zrekrutowano około 44 000 uczestników. Jednym z takich ośrodków była Ventavia Research Group, która prowadziła badania w 3 placówkach. Kierownikiem jednej z nich była Pani Brook Jackson, która była świadkiem, że firma fałszowała dane z badań klinicznych, „odślepiała” pacjentów (III faza badań to badania podwójnie zaślepione – ani pacjent ani lekarz nie wiedzą co jest podawane – lek czy placebo), zatrudniała nieodpowiednio przeszkolone osoby do wykonywania szczepień i nie reagowała na zdarzenia niepożądane zgłaszane w kluczowym etapie III fazy badań klinicznych firmy Pfizer. Mimo że Jackson wielokrotnie informowała Ventavię o problemach, firma nie podjęła żadnych działań naprawczych. To skłoniło Jackson do wysłania skargi do US Food and Drug Administration (FDA) - głównego organu regulacyjnego w kraju - we wrześniu 2020. Tego samego dnia Ventavia zwolniła Brook z pracy. Jackson dostarczyła jednak BMJ dziesiątki wewnętrznych dokumentów firmowych, zdjęć, nagrań audio i e-maili, które zdążyła zabezpieczyć przed zwolnieniem. W mailu do FDA Jackson informowała FDA, że wśród ponad 1000 uczestników badania (pełna próba zarejestrowana pod nr NCT04368728 obejmowała około 44 000 uczestników w 153 miejscach jak firmy komercyjne lub ośrodki akademickie) wychwyciła następujące problemy:
- brak zabezpieczenia danych pacjentów co mogło powodować odślepienie próby
- niezgłaszanie odstępstw od protokołu
- uczestnicy umieszczani w korytarzu po wstrzyknięciu i nie monitorowani przez personel kliniczny
- brak terminowej obserwacji pacjentów, u których wystąpiły zdarzenia niepożądane
- niewłaściwe przechowywanie odpadów po szczepieniach
- przechowywane szczepionek w nieodpowiedniej temperaturze
- niewłaściwie oznakowanie próbek laboratoryjnych
- spóźnione wprowadzanie danych, które powinny być procesowane w ciągu 24 godzin
Mimo, że problemy te ograniczają się do trzech z ponad 150 ośrodków badawczych, do których zapisano tylko 1000 z około 44 000 wszystkich uczestników, to jednak dane z Ventavii mogą mieć szersze konsekwencje, również dla danych dotyczących skuteczności szczepionek, bo jeśli wśród tych 170 osób z badania, które zachorowały na COVID były też osoby zrekrutowane przez Ventavię to może mieć to olbrzymi wpływ na końcowy wynik badania (sprawę Brook Jackson opisywał BMJ https://www.bmj.com/content/375/bmj.n2635).
Brook Jackson zdecydowała się wejść na drogę sądową z byłym pracodawcą za bezpodstawne zwolnienie oraz z firmą Pfizer.
Według prawników reprezentujących Brook, jest to najważniejsza sprawa dotycząca informatorów czy demaskatorów (whistleblowers) w historii – potencjalnie z 2,9 bilionami dolarów odszkodowania za oszustwo popełnione wobec społeczeństwa. Ta jedna sprawa może doprowadzić do bankructwa firmy Pfizer i zakłócić funkcjonowanie całego przemysłu farmaceutycznego oraz agencji regulacyjnych, które nie wywiązały się ze swoich zadań w zakresie nadzoru nad bezpieczeństwem. Brook Jackson złożyła pozew federalny w imieniu obywateli Stanów Zjednoczonych Ameryki, tak zwany False Claims Act (FCA). FDA robiła wszystko, aby opóźnić ten proces, teraz sprawa jest w rękach sędziego federalnego w Beaumont w Teksasie, który zdecyduje, czy sprawa będzie mogła być kontynuowana w celu przeprowadzenia badań, a także ustali datę rozprawy.
Źródła:
https://www.syncsci.com/journal/FMI/article/view/521/430
https://www.thelancet.com/action/showPdf?pii=S2666-5247%2821%2900069-0