Interpelacje poselskie w sprawie dopuszczenia do użycia Iwermektyny w Polsce
Analiza odpowiedzi Ministerstwa Zdrowia pokazuje, że czas na kolejną interpelację
Kolej rzeczy:
1. Pierwsza Interpelacja poseł Pępek z maja 2021 w sprawie Iwermektyny i odpowiedź z Ministerstwa Zdrowia
2. Druga Interpelacja poseł Pępek z sierpnia 2021 w sprawie Iwermektyny i odpowiedź z Ministerstwa Zdrowia
3. Analiza odpowiedzi Ministerstwa Zdrowia
4. Przykłady innych badań – nie uwzględnionych w odpowiedzi MZ
5. Dopuszczenie leku do obrotu w Polsce
6. Interpelacja o włączenie Iwermektyny do leczenia na wniosek pacjenta i przygotowania protokołu leczenia wstępnego
7. Odnośniki
1. Pierwsza Interpelacja poseł Pępek z maja 2021 w sprawie Iwermektyny i odpowiedź z Ministerstwa Zdrowia
15 kwietnia 2021 wpłynęła do ministra zdrowia interpelacja złożona przez poseł Małgorzatę Pępek w sprawie możliwości wprowadzenia na rynek polski leku iwermektyna o treści:
Szanowny Panie Ministrze!
Badania epidemiologiczne, obserwacyjne i randomizowane badania kliniczne kontrolowane wykazały, że iwermektyna jest wysoce skuteczna w profilaktyce poekspozycyjnej, profilaktyce przedekspozycyjnej oraz leczeniu tak na wczesnym, jak i późnym etapie COVID-19. Ten bezpieczny i tani lek może zmienić trajektorię pandemii. To jeden z najbezpieczniejszych, najlepiej przebadanych leków na liście najbardziej niezbędnych według Światowej Organizacji Zdrowa. Jako lek przeciwpasożytniczy jest w użyciu od czterech dekad i został podany ludziom miliardy razy. Jego efekty uboczne są dobrze znane i niewielkie. Obecnie lek ten został już wdrożony w leczeniu koronawirusa w dwudziestu krajach, między innymi takich jak Czechy i Słowacja, a także jest szeroko dystrybuowany w Bułgarii. W Polsce lek ten w ogóle nie jest dostępny dla społeczeństwa (oprócz kremu) nawet w jego funkcji pierwotnej - środka przeciwpasożytniczego.
Kierując pytania do Pana Ministra, proszę o odpowiedzi na nurtujące mnie zagadnienia:
1. Czy Ministerstwu Zdrowia znany jest lek o nazwie iwermektyna?
2. Czy patrząc na inne kraje, w których został wdrożony do leczenia COVID-19, istnieje szansa, że w Polsce również będzie używany w tym celu?
3. Jeśli rząd nie zakłada wprowadzenia na rynek polski tego leku, to czym argumentuje swoje stanowisko, jakie przeciwskazania ku temu widzi?
4. Jeśli planuje wprowadzić ten lek na rynek Polski, to kiedy to nastąpi?
Odpowiedzi na ręce Marszałek Sejmu oddzielił Maciej Miłkowski Podsekretarz Stanu: http://orka2.sejm.gov.pl/INT9.nsf/klucz/ATTC2WBVB/%24FILE/i22785-o1.pdf - gdzie m.in. możemy przeczytać, że:
Iwermektyna jest to lek przeciwpasożytniczy, którego stosowanie u ludzi ogranicza się w Polsce do chorób dermatologicznych, tj. leczenia trądziku różowatego, a lek występuje w postaci kremu (dopuszczenie do obrotu wydane przez Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych).
W związku z nowymi informacjami w dniu 4 lutego 2021 r. Agencja Oceny Technologii Medycznych i Taryfikacji opracowała również przegląd doniesień naukowych dla iwermektyny w leczeniu oraz profilaktyce COVID-19, który stanowił podstawę dyskusji Panelu Ekspertów Klinicznych. Na podstawie powyższego przeglądu Agencja przeprowadziła proces aktualizacji Zaleceń - Farmakoterapia COVID-19. Zgodnie z opinią grona ekspertów nie zaleca się rutynowego stosowania iwermektyny w leczeniu COVID-19. W podsumowaniu opracowania wskazano, że dowody naukowe na skuteczność iwermektyny nie są przekonujące i nie pozwalają na ostateczne wnioskowanie. Dostępne dane z badań klinicznych, pochodzące z innych krajów są w większości słabej jakości. Niektóre wskazują na brak skuteczności iwermektyny, inne na obniżenie stężenia wskaźników stanu zapalnego, skrócenie czasu eliminacji wirusa, ustępowanie objawów klinicznych oraz zmniejszenie śmiertelności. Ograniczenia metodyczne dostępnych badań to m.in.: brak zaślepienia, małe grupy chorych, różne dawki i sposoby podawania iwermektyny, stosowanie w grupach kontrolnych terapii nieskutecznych lub o udowodnionej szkodliwości w COVID-19, a także nieprecyzyjne określenie zaawansowania choroby i punktów końcowych. Jednocześnie Minister Zdrowia informuje, że pełna treść zalecenia dostępna jest na stronie internetowej:
https://www.aotm.gov.pl/media/2021/03/Farmakoterapia-COVID-19-Aktualizacjawersja-2.2-23-marca-2021-r..pdf (która nie istnieje)
W ostatniej aktualizacji do Rekomendacji możemy przeczytać (opinia ta została wydana w oparciu o „Przegląd doniesień naukowych dla iwermektyny w leczeniu oraz profilaktyce COVID-19” z dnia 21 maja 2021r. https://www.aotm.gov.pl/media/2021/05/Iwermektyna-w-COVID-19-Rapid-Review-aktualizacja-wersja-1.1-21-maja-2021-r..pdf):
W piśmie z ministerstwa zdrowia czytamy również, że:
„Wszystkie zalecenia opublikowane są na stronie internetowej: http://www.pteilchz.org.pl/informacje/rekomendacje/. W przypadku pojawienia się nowych dowodów, pochodzących z wiarygodnych prób klinicznych, powyższe zalecenia mogą ulec zmianie”. Jednocześnie podsekretarz podkreśla, że „Minister Zdrowia nie zabronił stosowania iwermektyny we wskazaniach pozarejestracyjnych. Zgodnie z art. 4 ustawy z dnia 5 grudnia 1996 r. o zawodach lekarza i lekarza dentysty (Dz. U. z 2021 r. poz. 790) lekarz ma obowiązek wykonywać zawód, zgodnie ze wskazaniami aktualnej wiedzy medycznej, dostępnymi mu metodami i środkami zapobiegania, rozpoznawania i leczenia chorób, zgodnie z zasadami etyki zawodowej oraz z należytą starannością. Zatem lekarz ma możliwość stosowania wśród pacjentów produktów leczniczych również w zakresie pozarejestracyjnym.”
2. Druga Interpelacja poseł Pępek z sierpnia 2021 w sprawie Iwermektyny i odpowiedź z Ministerstwa Zdrowia
W sierpniu 2021 Poseł Małgorzata Pępek kieruje kolejna interpelację poselską do MZ w sprawie wyjaśnienia wątpliwości dotyczących wprowadzenia na rynek polski leku iwermektyna:
Szanowny Panie Ministrze!
Po raz kolejny chciałam zwrócić uwagę Pana Ministra na możliwość wprowadzenia na rynek polski leku iwermektyna. W świetle istniejących badań specyfik ten możnaby stosować zarówno w leczeniu COVID-19, ale także w profilaktyce związanej z koronawirusem. Przemawia za tym szczególnie fakt, że w prawie dwudziestu państwach na świecie preparat ten jest stosowany jako lek na COVID-19, są to m.in. Stany Zjednoczone, Indie, Izrael, Czechy czy Słowacja.
W odpowiedzi na moją interpelację w tej sprawie zwracano uwagę, że lek ten jest rzekomo nieprzebadany, oraz że opinie na jego temat są rozbieżne w różnych kręgach naukowych. Dlatego właśnie kontrowersje budzi fakt, że Polska nie prowadzi nad nim badań, co czynią nasi sąsiedzi: Czesi i Słowacy.
Powołując się na konkretne dane, do mojego biura wpłynęło pismo od fundacji Pomarańczowa Alternatywa, w którym czytamy:
„Eksperci Agencji Oceny Technologii Medycznych i Taryfikacji już w lutym br. dysponowali wiedzą o minimum dwóch, a zasadzie trzech (2 x Elgazzar: leczenie i profilaktyka) RCT klasy „C” wg. AOTMiT, które w sposób statystycznie istotny wykazały korzyści ze stosowania iwermektyny w leczeniu COVID–19 oraz trzynastu klasy „E”, które także wykazały podobne korzyści”.W świetle wyżej przytoczonych informacji proszę Pana Ministra o odpowiedź na następujące pytania:
1. Dlaczego nie prowadzi się w Polsce badań klinicznych zmierzających do zezwolenia stosowania inwermektyny w leczeniu COVID-19?
2. Dlaczego wprowadzono na rynek leki przebadane w mniejszym stopniu np. budezonid, a inwermektyna pozostaje niedopuszczona?
3. Kiedy można spodziewać się ewentualnych decyzji ministerstwa w sprawie inwermektyny?
Odpowiedzi na interpelację ponownie udzielił Podsekretarz Stanu Maciej Miłkowski (https://orka2.sejm.gov.pl/INT9.nsf/klucz/ATTC6UH3Z/%24FILE/i26263-o1.pdf), w której m.in. czytamy, że:
„Dane dotyczące skuteczności leku pochodzą w zdecydowanej większości z prób klinicznych o niskiej wiarygodności (…). Wyniki dwóch badań o największej liczebności – Lopez-Medina 2021 oraz Vallejos 2021 – nie wykazały przewagi iwermektyny nad placebo. Wyniki 17 kontrolowanych prób klinicznych z randomizacją, w których iwermektyna stosowana była w postaci doustnej w monoterapii lub w skojarzeniu z tzw. opieką standardową, nie wykazały znamiennych statystycznie różnic w śmiertelności. W ramach punktów końcowych odnoszących się do stanu klinicznego pacjentów, tj. progresja choroby, wyzdrowienie, występowanie objawów, w większości badań nie odnotowano znamiennych statystycznie różnic. Wyłącznie w jednym badaniu (Chachla 2021) w grupie iwermektyny podawanej doustnie odnotowano znamienne statystycznie zmniejszenie odsetka pacjentów z objawami choroby oraz zwiększenie odsetka pacjentów zwolnionych z opieki ambulatoryjnej. Wyniki badania Aref 2021, przeprowadzonego z udziałem pacjentów z łagodnym nasileniem objawów wskazują, że zastosowanie iwermektyny w postaci wziewnej znamiennie statystycznie skróciło czas utrzymywania się gorączki oraz objawów ze strony układu oddechowego, takich jak kaszel, duszności i anosmia. Należy jednak zaznaczyć, że aktualnie nie ma innych badań potwierdzających skuteczność terapii wziewnej, natomiast badanie Aref 2021 obarczone jest licznymi ograniczeniami metodycznymi. Ponadto należy zwrócić uwagę, że:
• publikacja Elgazzar 2020 (pre-print), na którą Pani Poseł się powołuje, została wycofana w lipcu 2021 r.,
• w badaniu Mahmud 2021, na które Pani Poseł się powołuje, iwermektyna była stosowana w skojarzeniu z doksycykliną – z uwagi na powyższe nie jest możliwe wnioskowanie na temat skuteczności iwermektyny w monoterapii.
Odnosząc się do możliwości stosowania iwermektyny w profilaktyce rozwoju COVID-19 u pacjentów zainfekowanych SARS-CoV-2, wyniki badania Samaha 2021 wskazują, iż podanie pojedynczej doustnej dawki iwermektyny pacjentom bezobjawowym, zakażonym SARS-CoV-2, wiązało się z rzadszym występowaniem w trzeciej dobie objawów takich jak gorączka, anosmia, bóle mięśniowe i utrata smaku, w porównaniu do pacjentów otrzymujących witaminę C i cynk. Autorzy badania zestawili jednak w publikacji wyłącznie dane krótkoterminowe (po 3 dniach od potwierdzenia infekcji), tym samym istnieje niepewność czy zaobserwowane różnice w skuteczności utrzymają się w dłuższym okresie obserwacji, czy iwermektyna wyłącznie odsuwa w czasie wystąpienie objawów. W dwóch badaniach, w których iwermektyna była stosowana w ramach profilaktyki zakażeń SARS-CoV-2 u osób po kontakcie z zakażonym (Shouman 2020) i u zdrowych ochotników (Seet 2021), w grupach pacjentów otrzymujących iwermektynę odnotowano niższe odsetki pacjentów z objawami choroby.”
3. Analiza odpowiedzi z Ministerstwa Zdrowia
Bilans korzyści i ryzyka wynikający z odpowiedzi wygląda w sposób następujący:
Korzyści:
Chachla 2021 w grupie iwermektyny podawanej doustnie odnotowano znamienne statystycznie zmniejszenie odsetka pacjentów z objawami choroby oraz zwiększenie odsetka pacjentów zwolnionych z opieki ambulatoryjnej.
Aref 2021, przeprowadzonego z udziałem pacjentów z łagodnym nasileniem objawów wskazują, że zastosowanie iwermektyny w postaci wziewnej znamiennie statystycznie skróciło czas utrzymywania się gorączki oraz objawów ze strony układu oddechowego, takich jak kaszel, duszności i anosmia.
Samaha 2021 - podanie pojedynczej doustnej dawki iwermektyny pacjentom bezobjawowym, zakażonym SARS-CoV-2, wiązało się z rzadszym występowaniem w trzeciej dobie objawów takich jak gorączka, anosmia, bóle mięśniowe i utrata smaku, w porównaniu do pacjentów otrzymujących witaminę C i cynk.
W dwóch badaniach, w których iwermektyna była stosowana w ramach profilaktyki zakażeń SARS-CoV-2 u osób po kontakcie z zakażonym (Shouman 2020) i u zdrowych ochotników (Seet 2021), w grupach pacjentów otrzymujących iwermektynę odnotowano niższe odsetki pacjentów z objawami choroby
Ryzyka (a właściwie brak lub małe korzyści):
Lopez-Medina 2021 oraz Vallejos 2021 – nie wykazały przewagi iwermektyny nad placebo (… ale czy wykazały jej szkodliwość? Czy w obliczu pandemii, nie powinniśmy się chwytać wszystkich potencjalnych szans, a nie jednej – i to będącej w fazie badań klinicznych?)
Wyniki 17 kontrolowanych prób klinicznych – IVM w monoterapii lub w skojarzeniu z tzw. opieką standardową, nie wykazały znamiennych statystycznie różnic w śmiertelności (… nie wykazały pogorszenia sytuacji – czego wiec boimy się?)
Algazzar 2020 (pre-print), na którą Pani Poseł się powołuje, została wycofana w lipcu 2021
Pytanie: czy wobec powyższego uzasadnione wydaję się twierdzenie, że Iwermektyna może być niebezpieczna dla pacjenta czy może jedynie, że jej skuteczność nie jest w pełni potwierdzona? I czy zasadne jest nie rekomendowanie jej do użycia?
W dalszej części Pan Podsekretarz Miłkowski pisze:
„Aktualnie brak jest dostatecznie wiarygodnych dowodów naukowych przemawiających za skutecznością iwermektyny w leczeniu lub profilaktyce COVID-19 i za dopuszczeniem jej na terenie Rzeczpospolitej Polski w jakimkolwiek preparacie do stosowania w leczeniu lub profilaktyce COVID-19.”
Dodatkowo należy zaznaczyć, iż zalecenia Agencji Oceny Technologii Medycznych i Taryfikacji w zakresie stosowania iwermektyny są zbieżne z wytycznymi innych państw oraz instytucji międzynarodowych, w tym:
Światowej Organizacji Zdrowia – „Zaleca się, aby nie stosować iwermektyny u pacjentów z COVID-19 z wyjątkiem badania klinicznego”;
National Institutes of Health (Stany Zjednoczone) – „Nie ma wystarczających dowodów, aby Panel zalecał lub nie zalecał stosowania iwermektyny w leczeniu COVID19. Konieczne jest uzyskanie wyników z poprawnie zaprojektowanych i przeprowadzonych badań klinicznych o dostatecznej mocy statystycznej, aby zapewnić bardziej szczegółowe, oparte na dowodach dane dotyczące roli iwermektyny w leczeniu COVID-19.”
Association of the Scientific Medical Societies in Germany (Niemcy) – “Nie zaleca się podawania iwermektyny hospitalizowanym pacjentom z COVID-19”. Ponadto, warto również zwrócić uwagę, że iwermektyna w postaci doustnej nie jest lekiem zarejestrowanym przez Europejską Agencję Leków (EMA) do stosowania u ludzi, natomiast w Stanach Zjednoczonych lek jest dopuszczony do stosowania u ludzi jedynie w leczeniu chorób pasożytniczych.
Zweryfikujmy te informacje:
WHO – Iwermektyna, to lek, który od lat jest na liście leków podstawowych WHO (od 1988r) jako lek pasożytniczy o wysokim profilu bezpieczeństwa: na ok. 4 mld dawek w systemie http://www.vigiaccess.org/ zgłoszono od 1992 roku 6 199 niepożądanych odczynów na lek (porównując to ze zgłoszonymi przez niecały rok 3 155 004 Niepożądanymi Odczynami po szczepieniach C-19 to bardzo bezpieczny lek). Dla porównania – paracetamol ma zgłoszone 172 475 reakcje niepożądane – dane z bazy WHO
NIH – w zaleceniach (https://www.covid19treatmentguidelines.nih.gov/therapies/antiviral-therapy/ivermectin/ ) jest napisane:
„Nie ma wystarczających dowodów, aby panel ds. wytycznych dotyczących leczenia COVID-19 zalecił stosowanie lub niestosowanie iwermektyny w leczeniu COVID-19. Aby dostarczyć bardziej szczegółowe, oparte na dowodach naukowych wytyczne dotyczące roli iwermektyny w leczeniu COVID-19, potrzebne są wyniki odpowiednio zasilanych, dobrze zaprojektowanych i przeprowadzonych badań klinicznych. Jednocześnie w uzasadnienie możemy przeczytać, że „wyniki kilku badań randomizowanych i retrospektywnych badań kohortowych dotyczących stosowania iwermektyny u pacjentów z COVID-19 zostały opublikowane w recenzowanych czasopismach lub udostępnione jako manuskrypty przed recenzją. Niektóre badania kliniczne nie wykazały żadnych korzyści lub pogorszenie choroby po zastosowaniu iwermektyny, natomiast w innych odnotowano krótszy czas do ustąpienia objawów choroby, które przypisano COVID-19, większe zmniejszenie poziomu markerów stanu zapalnego, krótszy czas do usunięcia wirusa, lub mniejszą śmiertelność u pacjentów, którzy otrzymywali iwermektynę niż u pacjentów, którzy otrzymywali leki porównawcze lub placebo.”
Dodatkowo Ministerstwo Zdrowia nie wiedzieć czemu pomija załącznik w rekomendacjach Tabela 2e: Charakterystyka leków przeciwwirusowych, które są zatwierdzone lub oceniane w leczeniu COVID-19, w której widnieje Iwermektyna: https://www.covid19treatmentguidelines.nih.gov/tables/table-2e/
Niemieckie Association of the Scientific Medical Societies – nie zaleca stosowania iwermektyny ale zalecają ja inne stowarzyszenia i organizacje z całego świata jak np.:
- Association of American Physicians and Surgeons (AAPS) https://aapsonline.org/
- FLCCC Alliance https://covid19criticalcare.com/
- World Doctors Alliance - https://worlddoctorsalliance.com/
- Médicos pela Vida - https://medicospelavidacovid19.com.br
- Long Covid-19 Foundation - http://www.longcovidfdn.com/
- Covid Medical Network - https://covidmedicalnetwork.com/
- Canadian Covid Care Alliance - https://www.canadiancovidcarealliance.org/
- Transformative Health Justice (THJ) - https://thj-africa.org.za
- Doctors for Covid Ethics - https://doctors4covidethics.org/
- Association BonSens - https://bonsens.info/
- Alliance for Natural Health International - https://www.anhinternational.org/
- CetiCov19 - https://www.ceticov19.org/
- Physicians for Informed Consent - https://physiciansforinformedconsent.org/
- International Covid Summit - https://www.internationalcovidsummit.com/
- IppocrateOrg.org - https://ippocrateorg.org/en/
- Concerned Doctors & Citizens of the Philippines - https://cdcph.org/
- Malaysian Association for Advancement of Functional and Interdisciplinary Medicine - http://maafim.org/
- PANDA - Pandemics - Data & Analytics - https://www.pandata.org/
- Society for Advancement of Hormones & Healthy Aging Medicine Malaysia -
- United Health Alliance - https://world-harmony.wixsite.com/united-health/home
oraz wiele innych organizacji jak: Organización Mundial Por La Vida (World Life Organisation), Indian Nutritional Medical Association, Malaysian Alliance for Effective Covid Control – MAECC, Society for Regenerative, Anti-Ageing and Aesthetic Medicine – India, Functional Medicine Indonesia, International Anti-Aging And Integrative Medicine, Perhimpunan Dokter Umum Indonesia, Philippine Society for Orthomolecular Medicine, Plataforma Cartucho, Iniciativa slovenskih zdravnikov, Conscious Health Grenada
4. Przykłady innych badań – nie uwzględnionych w odpowiedzi z Ministerstwa Zdrowia
Czy wybiórcze cytowanie pojedynczych przykładów badań nie jest próba dopasowania danych pod założoną tezę? Bo tak to wygląda, gdyż istnieją 32 badania (tzw. Golden standard – badania RCT) które dowodzą 62% skuteczności przy stosowaniu iwermektyny w leczeniu wstępnym, 23% w leczeniu późnym i 84% przy profilaktyce.
Poproszę o wyjaśnienie czemu Pan Podsekretarz Stanu nie odnosi się do wielu kontrolowanych, randomizowanych i recenzowanych badań czy przeglądów systematycznych, jak chociażby przytoczone poniżej:
1/ Lucy Kerr, Flavio A. Cadegiani https://www.cureus.com/articles/82162-ivermectin-prophylaxis-used-for-covid-19-a-citywide-prospective-observational-study-of-223128-subjects-using-propensity-score-matching - najnowsze, olbrzymie recenzowane studium badawcze z Brazylii dowodzi, że regularne stosowanie iwermektyny jako profilaktyki wiązało się z istotnie niższymi wskaźnikami zakażeń COVID-19, hospitalizacji i śmiertelności – badaniu poddana została cała populacja brazylijskiego Itajaí, miasta portowego w stanie Santa Catarina. Spośród 223 128 mieszkańców Itajaí, którzy wzięli udział w badaniu, w sumie 159 561 osób zdecydowało się wziąć w nim udział: ponad 70% zdecydowało się przyjmować iwermektynę, a 23% nie zdecydowało się na to. Badanie wykazało 44% redukcję liczby infekcji COVID-19 na korzyść grupy, która przyjmowała iwermektynę (3,5% w porównaniu do 8,2%), a regularne stosowanie profilaktycznej iwermektyny doprowadziło do 68% redukcji śmiertelności w grupie COVID-19 (0,8% w porównaniu z 2,6%) oraz 56% redukcji liczby hospitalizacji (1,6% w porównaniu z 3,3%).
2/ przegląd systematyczny, metaanaliza i analiza sekwencyjna badań, dokonana przez Instytut Nauk o Zdrowiu Populacji i Evidence-based Medicine Consultancy, opublikowana w czerwcu 2021 (Ivermectin for Prevention and Treatment of COVID-19 Infection: A Systematic Review, Meta-analysis, and Trial Sequential Analysis to Inform Clinical Guidelines https://www.ncbi.nlm.nih.gov/labs/pmc/articles/PMC8248252/), badania , którego konkluzja brzmi: „dowody o umiarkowanej pewności wskazują na możliwość znacznego zmniejszenia liczby zgonów z powodu COVID-19 przy zastosowaniu iwermektyny. Zastosowanie iwermektyny na wczesnym etapie przebiegu klinicznego może zmniejszyć liczbę osób przechodzących w ciężką postać choroby. Widoczne bezpieczeństwo i niski koszt sugerują, że iwermektyna może mieć znaczący wpływ na pandemię SARS-CoV-2 na całym świecie”.
3/ Ahmed, International Journal of Infectious Diseases, https://doi.org/10.1016/j.ijid.2020.11.191 (recenzowane) „Pięciodniowy kurs iwermektyny w leczeniu COVID-19 może skrócić czas trwania choroby”
4/ Chaccour, EClinicalMedicine, https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(20)30464-8/fulltext (recenzowane) “Wpływ wczesnego leczenia iwermektyną na wiremię, objawy i odpowiedź humoralną u pacjentów z nieciężką postacią COVID-19: Pilotażowe, podwójnie ślepe, kontrolowane placebo, randomizowane badanie kliniczne”
5/ Babalola, An International Journal of Medicine, https://academic.oup.com/qjmed/advance-article/doi/10.1093/qjmed/hcab035/6143037 (recenzowane) “Iwermektyna wykazuje korzyści kliniczne w łagodnej do umiarkowanej postaci COVID19: randomizowane, kontrolowane badanie z podwójnie ślepą próbą, z odpowiedzią na dawkę, przeprowadzone w Lagos”
6/ Ravikirti, Journal of Pharmacy & Pharmaceutical Sciences, https://journals.library.ualberta.ca/jpps/index.php/JPPS/article/view/32105, (recenzowane), „Iwermektyna jako potencjalne leczenie łagodnej do umiarkowanej postaci COVID-19: Podwójnie ślepe, randomizowane badanie kontrolowane placebo”.
7/ Mohan, Journal of Infection and Chemotherapy, https://www.jiac-j.com/article/S1341-321X(21)00239-7/fulltext (recenzowany) “Pojedyncza dawka doustnej iwermektyny w łagodnej i umiarkowanej postaci COVID-19 (RIVET-COV): jednoośrodkowe randomizowane badanie kontrolowane placebo”.
8/ López-Medina, JAMA, https://jamanetwork.com/journals/jama/fullarticle/2777389 (recenzowany) „Wpływ iwermektyny na czas do ustąpienia objawów wśród dorosłych z łagodną postacią COVID-19: Randomizowane badanie kliniczne”.
9/ Faisal, The Professional Medical Journal, http://theprofesional.com/index.php/tpmj/article/view/5867 (recenzowane) “Potencjalne zastosowanie azytromycyny samej oraz w połączeniu z iwermektyną w zwalczaniu objawów COVID-19”.
10/ Krolewiecki, EClinicalMedicine, https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(21)00239-X/fulltext (recenzowane) „Przeciwwirusowe działanie wysokich dawek iwermektyny u dorosłych chorych na COVID-19: Badanie randomizowane typu proof-of-concept”.
5. Dopuszczenie leku do obrotu w Polsce
Pan Podsekretarz w dalszej części odpowiedzi informuje, że:
„W nawiązaniu do pytania w zakresie dopuszczenia do obrotu iwermektyny na terenie Rzeczpospolitej Polski, uprzejmie informuję, że postępowania w przedmiocie dopuszczenia do obrotu produktów leczniczych nie są postępowaniami wszczynanymi przez organ z urzędu. Postępowania te są postępowaniami wnioskowymi, wszczynanymi przez podmiot odpowiedzialny. Zasada ta dotyczy wszystkich postępowań rejestracyjnych: procedury centralnej uregulowanej w rozporządzeniu Parlamentu Europejskiego i Rady (WE) Nr 726/2004 z dnia 31 marca 2004 r. ustanawiającego unijne procedury wydawania pozwoleń dla produktów leczniczych stosowanych u ludzi i nadzoru nad nimi oraz ustanawiające Europejską Agencję Leków (Dz. Urz. UE L Nr 136 str. 1, z późn. zm.) oraz uregulowanych w ustawie z dnia 6 września 2001 r. Prawo farmaceutyczne (Dz. U. z 2021 r. poz. 974, z późn. zm.) procedur: zdecentralizowanej, wzajemnego uznania i procedury narodowej. Ponadto do wniosku konieczne jest dołączenie dokumentacji potwierdzającej jakość, skuteczność i bezpieczeństwo produktu leczniczego, o którego dopuszczenie do obrotu ubiega się wnioskodawca. W związku z powyższym decyzja o wystąpieniu z wnioskiem o dopuszczenie do obrotu produktu leczniczego należy do podmiotu odpowiedzialnego. Jednocześnie nowe substancje czynne stosowanie w chorobie wirusowej wywołanej SARS-CoV-2 rejestrowane są w procedurze centralnej. W przypadku tej procedury wniosek o dopuszczenie do obrotu rozpatrywany jest przez Europejską Agencję Leków (EMA – European Medicines Agency), natomiast decyzję w tej sprawie wydaje Komisja Europejska na podstawie opinii naukowej Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP).”
Na jakiej więc podstawie dopuszczono w Polsce do użytku lek pod nazwą POSELA (https://www.lekinfo24.pl/lek/Posela.html) oferowany przez firmę Substipharm-Developpement produkującą „niszowe produkty generyczne”?
Skoro – jak Pan Podsekretarz argumentuje - „nowe substancje czynne stosowanie w chorobie wirusowej wywołanej SARS-CoV-2 rejestrowane są w procedurze centralnej. W przypadku tej procedury wniosek o dopuszczenie do obrotu rozpatrywany jest przez Europejską Agencję Leków (EMA – European Medicines Agency), natomiast decyzję w tej sprawie wydaje Komisja Europejska na podstawie opinii naukowej Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP)” to jak wyjaśnić fakt, że lek Iwermektyna (pod nazwą Stromectol, Huvemec, Ivermectine) jest dopuszczony do obrotu w wyszczególnionych poniżej krajach? Czy jest to wynik autoryzacji EMA czy autonomiczna decyzją rządów państwa członkowskich?
- Niemczech (https://www.german-apotheke.de/stromectol-kaufen.html ),
- na Słowacji (https://spectator.sme.sk/c/22583299/use-of-parasite-medication-to-treat-coronavirus-patients-approved-in-slovakia.html ),
- w Bułgarii (https://www.aptekadetelina.bg/huvemec-3-mg-ivermectin-hyuvemek-3-mg-ivermektin-30-tabletki ; https://www.economic.bg/web/files/richeditor/marketing-authorization-ial.pdf )
- w Czechach (https://trialsitenews.com/czech-ministry-of-health-officially-authorizes-temporary-use-of-ivermectin-due-to-covid-19-crisis/ )
- w Portugalii (https://trialsitenews.com/czech-ministry-of-health-officially-authorizes-temporary-use-of-ivermectin-due-to-covid-19-crisis/ )
Dodatkowo, na stronach EMA widnieje informacja, że iwermektyna to „lek zatwierdzany w procedurze narodowej” – czy zatem Pan Podsekretarz mija się z prawdą, czy brak mu wiedzy?
7. Interpelacja o włączenie Iwermektyny do leczenia profilaktycznego i wstępnego na wniosek pacjenta oraz o przygotowanie protokołu leczenia wstępnego
Walka o stosowanie w leczeniu C-19 dopuszczonego dziesięciolecia temu leku, który ma bardzo wysoki profil bezpieczeństwa zaczyna ocierać się o groteskę.
W Naperville w stanie Illinois w USA, rodzina wygrała batalię prawną o zgodę na podawanie iwermektyny 71-letniemu mężczyźnie, który od 19 października był podłączony do respiratora. Mężczyzna przyjechał z Hong Kongu do Chicago, aby odwiedzić swoją córkę. Zachorował na COVID i w ciągu kilku dni wylądował pod respiratorem w Edward Hospital w Naperville. Jego córka zdesperowana, chciała, aby szpital wypróbował iwermektynę, ale odmówiono jej na podstawie różnych krajowych wytycznych medycznych, które sugerują, że lek ten jest nieskuteczny. Sędzia hrabstwa DuPage orzekł na korzyść rodziny, nakazując szpitalowi zezwolić na podawanie leku – argumentując, że skoro pacjent jest praktycznie na łożu śmierci, podanie iwermektyny nie pogorszy tej sytuacji w żaden sposób. Pacjentowi podano dziennie 24 miligramów iwermektyny od 8 do 12 listopada. 27 listopada pacjent został wypisany do domu.
W USA tego typu przykładów jest wiele – za każdym razem, pacjenci, którym podano iwermektynę po nakazie sądowym wracali do zdrowia.
Retargetowanie istniejących leków jest normą w leczeniu nowych chorób. W maju 2020 r Narodowe Centrum Nauki (państwowa agencja wykonawcza podlegająca Ministerstwu Nauki i Szkolnictwa Wyższego @NCN_PL) w ekspresowym tempie przyznało 19 mln PLN na wsparcie wyłonionych w konkursie projektów badań nad Covid-19.
Jednym z projektów objętych finansowaniem było badanie „Retargetowanie znanych leków w kierunku proteaz uczestniczących w rozwoju choroby COVID-19”, prowadzone pod kierownictwem Prof. Marcina Drąga z Politechniki Wrocławskiej (kwota dofinansowania 1 590 000 zł).
Celem projektu było „przeszukanie biblioteki kilku tysięcy zaakceptowanych przez amerykańską Agencję Żywności i Leków i inne agencje leków wobec pięciu proteaz (ACE2, TMPRSS2, katepsyn B i L, SARS-CoV-2-PLpro) w celu znalezienia cząsteczek, które mogą hamować którąkolwiek z tych proteaz zaangażowanych w inwazję SARS-CoV-2 i rozwój COVID-19. Identyfikacja takich cząsteczek natychmiast dostarczy informacji o kandydatach do retargetowania leków”. Kiedy poznamy wyniki badań? Inhibitorem proteaz jest nowy, tymczasowo dopuszczony do użytku lek firmy Pfizer – Paxlovid, łączony ze starym lekiem na HIV – Ritonawirem, lek w tabletkach, który stosowany ma być w leczeniu wstępnym.
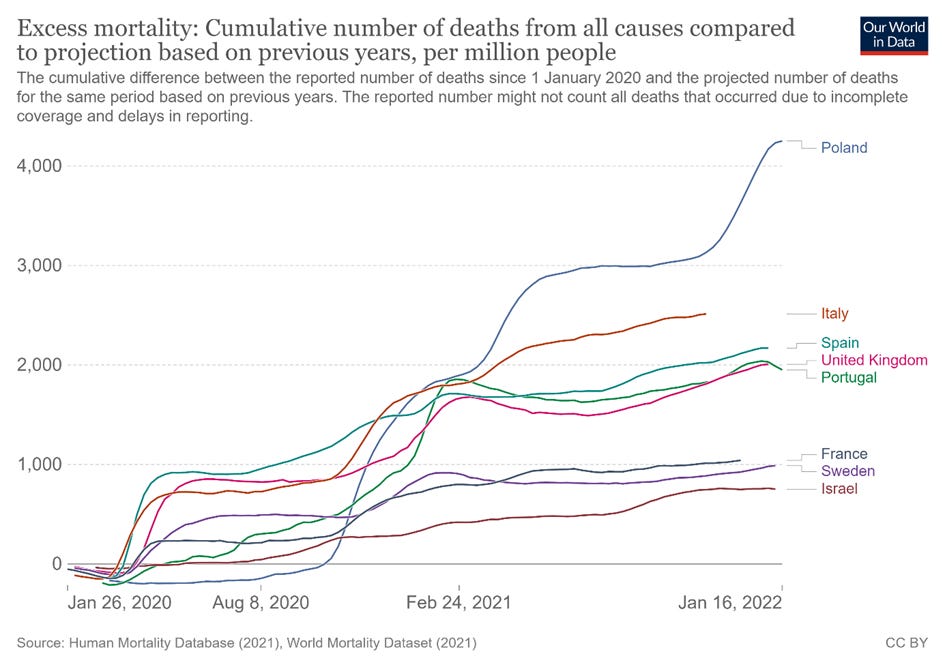
Polska – jak wynika z wykresu (dane za ourworldindata.org/covid-vaccinations) zajmuje niechlubne miejsce wśród Państw z nadmiarową liczba zgonów:
W obliczu masowych nadmiarowych zgonów Polaków, które spowodowane są wieloma czynnikami (zarządzanie kryzysem pandemicznym, utrudniony dostęp do służby zdrowia oraz brak jakichkolwiek protokołów leczenia wstępnego COVID-19) wnoszę o dopuszczenie iwermektyny do leczenia wstępnego COVID-19 na życzenie pacjenta oraz o wypracowanie algorytmu leczenia wstępnego, który będzie opierał się o analizę istniejących na świecie protokołów jak:
- Early Ambulatory Multidrug Therapy, McCullough https://rcm.imrpress.com/article/2020/2153-8174/RCM2020264.shtml
- I-MASK+ Protokół leczenia wczesnego i ambulatoryjnego dla pacjentów z COVID-19 https://covid19criticalcare.com/wp-content/uploads/2021/04/FLCCC_Alliance-I-MASKplus-Protocol-POLSKI-Polish.pdf
- MATH+ - Protokół szpitalnego leczenia Covid-19 https://covid19criticalcare.com/wp-content/uploads/2021/04/FLCCC-Alliance-MATHplus-Protocol-POLSKI-Polish.pdf
- I-RECOVER Protokół postępowania w zespole post Covid-19 https://covid19criticalcare.com/wp-content/uploads/2021/07/FLCCC_Alliance-I-RECOVER-Post-COVID19-Protocol-Polski-Polish.pdf
- Protokół AAPS - https://aapsonline.org/covidpatientguide/
- zalecenia indyjskiego Ministerstwa Zdrowia - https://www.mohfw.gov.in/pdf/RevisedguidelinesforHomeIsolationofmildasymptomaticCOVID19cases.pdf
6. Odnośniki
1. Interpelacja nr 22785 w sprawie możliwości wprowadzenia na rynek polski leku iwermektyna https://www.sejm.gov.pl/sejm9.nsf/interpelacja.xsp?documentId=349A2C10666F9363C12586B9004B2C00
2. Interpelacja nr 26263 w sprawie wyjaśnienia wątpliwości dotyczących wprowadzenia na rynek polski leku iwermektyna https://www.sejm.gov.pl/sejm9.nsf/interpelacja.xsp?documentId=D9E92612094D8120C125872E003EF914&view=S
- standardy i wytyczne Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych http://www.pteilchz.org.pl/informacje/rekomendacje/
- Zalecenia postępowania w zakażeniach SARS-CoV-2 Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych wersja 31-03-2020 http://www.pteilchz.org.pl/wp-content/uploads/2020/05/Prof.Flisiak_2020-PAIM-COVID-19-recommendation-PTEiLChZ-pl.pdf
- Aneks nr 1 z 08-06-2020 do Zalecenia postępowania w zakażeniach SARS-CoV-2 Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych http://www.pteilchz.org.pl/wp-content/uploads/2020/07/COVID-19-PTEiLChZ-2020-Anex-1-wersja-polska.pdf
- Aneks #2 do rekomendacji z 31 marca 2020 http://www.pteilchz.org.pl/wp-content/uploads/2020/10/Aneks-2-do-Rekomendacji-PTEiLChZ-13-10-2020-pl.pdf
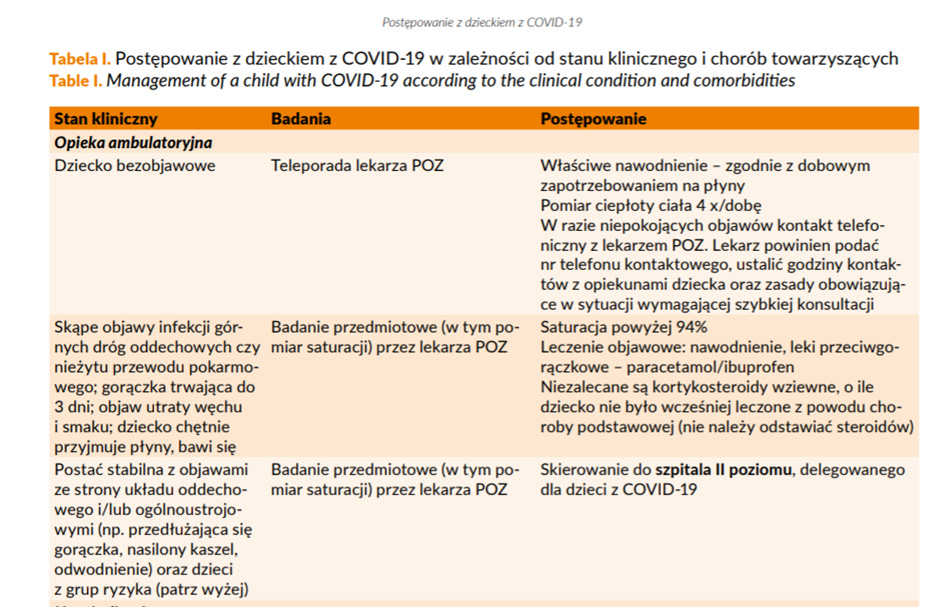
- Zalecenia dla pediatrów oraz lekarzy medycyny rodzinnej w podstawowej opiece zdrowotnej oraz dla leczących dzieci zakażone SARS-COV-2 w warunkach szpitalnych http://www.pteilchz.org.pl/wp-content/uploads/2021/04/Post%C4%99powanie-z-dzieckiem-z-C19-Przegl%C4%85d-Pediatryczny-2020.pdf
- Agencja Oceny Technologii Medycznych i Taryfikacji - Farmakoterapia COVID-19 – Aktualizacja z dnia 14.10.2021 r. https://www.aotm.gov.pl/media/2021/10/Farmakoterapia-COVID-19-Aktualizacja-wersja-2.9-14.10.2021.pdf
- Opracowanie analityczne AOTMiT -Przegląd doniesień naukowych dla iwermektyny w leczeniu oraz profilaktyce COVID-19 https://www.aotm.gov.pl/media/2021/05/Iwermektyna-w-COVID-19-Rapid-Review-aktualizacja-wersja-1.1-21-maja-2021-r..pdf, https://www.aotm.gov.pl/media/2021/08/Iwermektyna-w-COVID-19-Rapid-Review-wersja-1.2-6-sierpnia-2021-r..pdf
- W 2020 roku dr. Pierre Kory został zaproszony do złożenia zeznań przed Senacką Komisją ds. Bezpieczeństwa Wewnętrznego i Spraw Rządowych w sprawie leczenia, które on i jego koledzy z sojuszu FLCCC stosowali z powodzeniem i rekomendowania władzom ds. zdrowia i innym pracownikom medycznym zastosowania w walce z pandemią koronawirusa – przesłuchania odbyły się w maju i grudniu 2020 (https://covid19criticalcare.com/pl/zeznanie-senatu/).
- W grudniu FLCCC opublikowała „Przegląd pojawiających się dowodów wskazujących na skuteczność iwermektyny w profilaktyce i leczeniu COVID-19” (https://covid19criticalcare.com/wp-content/uploads/2021/04/OPS-Iwermektyna-w-leczeniu-COVID-19-%E2%80%93-kro%CC%81tki-przegla%CC%A8d-dowodo%CC%81w-klinicznych-POLSKI-Polish.pdf).
Przesłuchanie przed komisją oraz przegląd zainspirował dr. Theresa A. Lawrie do podjęcia próby szybkiego przeglądu i meta-analizy istniejących badań w celu sprawdzenia czy iwermektyna może być skutecznym lekiem na Covid-19 (https://www.ncbi.nlm.nih.gov/labs/pmc/articles/PMC8248252/)
- 19 listopada 2020 r. dr McCullough zeznawał w Komisji Bezpieczeństwa Wewnętrznego i Spraw Rządowych Senatu USA, a w roku 2021 w Komisji Zdrowia i Usług Społecznych Senatu Teksasu, Zgromadzeniu Ogólnym Kolorado i Senacie New Hampshire na temat wielu aspektów odpowiedzi na pandemię. Dr McCullough poświęcił się wysiłkom akademickim i klinicznym w walce z wirusem SARS-CoV-2, a w tym czasie przejrzał tysiące raportów, uczestniczył w kongresach naukowych, dyskusjach grupowych, publikacjach prasowych i został uznany za jednego ze światowych ekspertów w dziedzinie COVID-19, opublikował ok 50 prac badawczych dotyczących COVID-19, stworzył pierwszy protokół leczenia wstępnego - https://odysee.com/@PandemicParallaxView:6/DrMcCulloughTestimonySenateHearingC19OutpatientTreatment:e ,
,